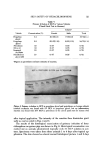
OXIDATION DYES 137 gruppe eine hypsochrome Bandenverschiebung bei gleichzeitiger Depression der Extinktionen rest. Dies hat offensichtlich seinen Grund darin, dat• die Struktur II im Grundzustand immer mehr •iberwiegt. Diese Anschauung kann durch folgendes Experiment erhiirtet werden. LSst man die Farbstoffe (Spektren in den Abbildungen 6 und 7) in einer Mischung aus Alkohol und Wasser 1: 1 und erhitzt sie wiihrend einer Stunde auf 100 ø C, so zeigt das Di•nnschicht-Chromatogramm die Bildung steigender Mengen Phenazin an, je liingerwellig ein Farbstoff dieser Gruppe absorbiert. Diese Regel gilt bei dieser Farbstoffgruppe allgemein. Je anteiliger die meso- mere Grenzstruktur I am Gesamtzustand ist, desto kleiner ist die Aktivie- rungsenergie der Addition der Aminogruppe an das chinoide Bindungssystem yon Iund desto grSfier ist die Geschwindigkeitskonstante dieser Reaktion. Sie wird im Folgenden noch einmal dargestellt (Abbildung 8). Reaktionsschritt 1: •"'•N•R2 •",,• N ,,•.• R 2 H + R 1 + I I I[ ] "--"R1 I LH [ i R't,'N"",,/H2N•N.2 H Reaktionsschritt 2: /'"•, N',•R2 + f,,"'• N•R 2 E•:,J...•A..J-,H 2 RI •1 RI' _ •N•R2 •N•R2 P•azin Leuko-Verbindung %-.-c.-oc• Ein Farbstoff der diskutierten Gruppe ist einer direkten Synthese in ana- lysenreiner Form auf dem yon Witt aufgezeigten Wege ni&t zug•ngli&. Es gelingt ni&t, das Reaktionsprodukt aus salzsaurem p-Nitrosoanilin mir 1.3- Diaminobenzol zu isolieren. Hier half folgender Kunstgriff weiter, der in Formeln wiedergegeben ist (Abbildung 9). Abbildung 9
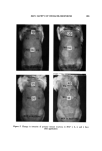
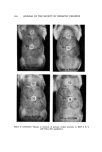
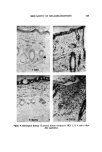
138 JOURNAL OF THE SOCIETY OF COSMETIC CHEMISTS Setzt man das 1.4-Diaminobenzol mit 1-Chlor-2.4-dinitrobenzol um, so erh•ilt man das 4-Amino-2'.4'-dinitrodiphenylamin. Diese Verbindung kann in absolutem Alkohol in Gegenwart von Platin aus Platinoxid (Adams) zur Leukoverbindung des gesuchten Farbstoffs reduziert werden. Anschliegende Luffoxidation fiihrt zu einer tiefblauen, optisch klaren L/Ssung, deren Spek- trum nach Einstellung des Oxidationsgleichgewichtes aufgenommen wurde. Das Spektrum besitzt in allen wesentlichen Merkmalen iiugerste Ahnlichkeit mit dem des Farbstoffes, der aus der Umsetzung yon salzsaurem p-Nitroso- anilin und 1.3-Diamino-4-methylbenzol gewonnen wurde. Der nicht kern- substituierte Farbstoff unterscheidet sich in der Bande maximaler Absorption nur um 2 nm in Richtung auf gr6gere Wellenliingen, ansonsten verlaufen bei logarithmischer Auftragung der Absorptionskurven dieselben praktisch par- allel. An einer analogen Struktur kann nicht gezweifelt werden. Auch wurden die Chromatogramme der synthetisch dargestellten Farb- stoffe mit denen der unter haarfiirberischen Bedingungen hergestellten Farb- stoffe sowohl einzeln als auch in Mischung miteinander verglichen. Es ergab sich voile Identitiit. Der Prozeg der Farbstoffbildung im Haar liigt sich wie folgt beschreiben: Das 1.4-Diaminobenzol dringt in ammoniakalisch-wiigrigem Medium in das Haar ein, wird durch das Wasserstoffperoxid zum Chinondiimin dehy- driert und kuppelt in Gegenwart yon Derivaten des 1.3-Diaminobenzols zu Farbstoffen vom Toluylenblautypus. Die Farbstoffe sind ionogen und sterisch aufgrund der Molekiilvergr6gerung an das Keratin gebunden. Strukturen vom Polyphenazintypus konnten nicht nachgewiesen werden. ZUSAMMENFASSUNG Es wird die Reaktion yon 1.4-Diaminobenzol mit Derivaten des 1.3-Dia- minobenzols in wiigrig-ammoniakalischen, wasserstoffperoxidhaltigen L6- sungen untersucht. Das primiir gebildete Chinondiimin kuppelt mit den Komponenten zu Farbstoffen vom Typus des yon O. N. Witt entdeckten Toluylenblaus. Durch systematischen Substituentenaustausch wurde die ge- samte Farbstoffgruppe synthetisiert. Aus dem spektralen Verhalten und aus den Geschwindigkeitskonstanten ihrer Oxidation zu Phenazinen bei erh6h- ter Temperatur konnten interessante Einblicke in die Lage der Mesomerie- Grundzustiinde gewonnen werden.
Purchased for the exclusive use of nofirst nolast (unknown) From: SCC Media Library & Resource Center (library.scconline.org)