j. Soc. Cosmet. Chem., 36, 381-391 (November/December 1985) Synthesen in der Isocamphanreihe. XXV. (Jber den Geruchseindruck von endo-konfigurierten Isocamphanderivaten* *R. VITEK und G. BUCHBAUER, lnstitut fi•'r Pharmazeutische Chemie der Universita't Wien, Wa'hringerstrasse A-1090 Vienna, Austria. Received September 3, 1985. Synopsis A total of 55 endo configured isocamphane derivatives was studied in order to establish a correlation between the shape of the molecule and its odor as postulated by the theory of Amoore. The molecules were measured by use of the shadow matching method and compared with cineole, the camphoraceous odor standard. The agreement of the results of these measurements with other molecular parameters, e.g. boiling point, was also examined. There is no pronounced difference between exo and endo epimers even though there could be detected some different new odor nuances, mainly earthy notes, exhibited by a few endo configured alcohols. In einer friiheren Mitteilung (1) berichteten wir fiber den Geruchseindruck von exo- konfigurierten Isocamphanderivaten und konnten feststellen, dab die kleineren und vor allem kugelig geformten Molekiile dieser Reihe einen camphrigen Geruchseindruck hervorrufen und dieser mit zunehmender Gri513e und somit st•irker asymmetrischer Gestalt der Molekiile abnimmt. Diese Befunde standen in Einklang mit der stereochemi- schen Geruchstheorie von A m o o r e (2). Es wurden damals (1) 55 exo-konfigurierte Isocamphanderivate vermessen und ihr Ge- ruchseindruck mit jenem der zwei fiir die Primiirgeriiche "camphrig" und "blumig" charakteristischen Standardverbindungen Cineol (12) und Phenylmethylpentanol (•9) im Schattenkorrelationstest nach A m o o r e verglichen. Die Ergebnisse der Vermes- sungen wurden statistisch ausgewertet und im t-Test nach S t u d e n t (3) auf ihre Signifikanz gepriift. Es wurde festgestellt, dab Molvolumen, Molekulargewicht und Siedepunkt der Verbindungen in Beziehung zu den Unterschieden der Schattenbilder im Schattenkorrelationstest stehen. Die Irrtumswahrscheinlichkeit, dab diese Ergebnisse zuf•illig waren, betrug bei allen Korrelationen weit unter 1%. Fiir die exo-konfigu- rierten Verbindungen war der Obergang von "camphrig" zu "blumig" bei einer Anzahl von 3 Kohlenstoffen in der Seitenkette zu beobachten. Sowohl die Beladung mit schweren Atomen als auch die Substitution mit osmophoren Gruppen •inderte nur die Nuance des Geruchseindruckes, nicht jedoch den "Prim•irgeruch". Schon damals aber bestand der Plan, diese Studie nicht nur auf die leichter zug•ingli- * Aus der Dissertation von R. Vitek, Universitit Wien, 1983. 381
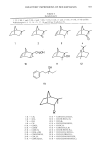
382 JOURNAL OF THE SOCIETY OF COSMETIC CHEMISTS chen exo-konfigurierten Isocamphane zu beschr•inken, sondern auch die entsprechenden epimeren endo-Verbindungen dem A m o o r e ' schen Schattenkorrelationstest zu unterwerfen. Ausgehend von der Camphenilans•iure (•6) (4) konnte vor kurzem erstmals eine Reihe neuer, epimerenreiner, endo-konfigurierter Isocamphanderivate dargestellt werden (5). Es schien daher interessant diese neuen Isocamphanverbindungen nun mittels des Schattenkorrelationstestes miteinander zu vergleichen und die Abh•ingigkeit des Ge- ruchseindruckes von der r•iumlichen Gestalt zu tiberprtifen. Es sollte untersucht werden, ob die stereochemische Theorie von A m o o r e auch ftir die Geruchsein- drticke der in Tabelle I angeftihrten endo-konfigurierten Isocamphanderivate gtiltig ist. Auf3erdem sollte in diesem Zusammenhang festgestellt werden, ob der 13bergang von "camphrig" zu "blumig", wie bei den exo-Verbindungen bei einer Anzahl von 3 Koh- lenstoffatomen in der Seitenkette zu beobachten ist, oder ob sich dieser infolge der andersartigen Raumausdehnung der Molektile •indert. Da der Wechsel des Geruchsein- druckes offensichtlich durch die elliptische Verzerrung der Molektilgestalt zustande kommt, stellte sich n•imlich die Frage, ob infolge der kompakteren Molektilform der endo-Verbindungen (durch die endo-Stellung der Seitenkette am C-2 wtirde auch bei Zunahme der Anzahl der C-Atome die kugelige Gestalt langer erhalten bleiben) der Obergang in den "blumigen Geruchsbereich" nicht etwa bei einer h6heren Anzahl der C-Atome in der Seitenkette erfolgen wtirde. MATERIAL UND METHODIK Zur Untersuchung kamen die in Tabelle 1 angefiihrten Isocamphanverbindungen, wobei 2, 3, 5, 10, 11 und einige Norisocamphane (1, 4, 6, 7) wie bei Lit. (1) aus Griinden der Vollstiindigkeit miteinbezogen wurden. Zum Bau der Molekiilmodelle wurden S t u a r t - B r i e g 1 e b 'sche Kalottenmo- delle der Firma L e y b o 1 d - H e r a e u s , K61n, verwendet. In ANinderung der "shadow-matching-method" (2) wurden siimtliche Molekiilmodelle direkt und nicht ihr Schatten fotografiert. Durch die Beleuchtung mir 2 ) 150 Watt Fotolampen war aber gewiihrleistet, dab der UrnriB des Bildes genau dem Schatten des Objektes entsprach. Die Modelle wurden aus drei verschiedenen, aufeinander senkrecht stehenden Rich- tungen mir einer Olympus Karoera OM 2n, mir Blende 22, Automatik, Entfernung 1 m und mir einem SchwarzweiBfilm ILFORD FP 4 mir DIN 18 aufgenommen. Um die Molekiilmodelle exakt fbtografieren zu k6nnen, war es notwendig, sie mir kleinen Sty- roporstiickchen zu stiitzen. Molekiile mir einem liingeren aliphatischen Rest wurden zum Fotografieren in der sterisch am wenigsten behinderten Form angeordnet. AuBerdem wurde darauf geachtet, dab sich die einzelnen Wasserstoffatome in gestaf- felter Stellung zueinander befanden, in der Annahme, dab dies die wahrscheinlichste Molekiilform ist. Die Aufnahmen wurden so vergr6Bert, dab das mitfotografierte Millimeterpapier wieder der natiirlichen Gr6Be entsprach. Nach Angaben der Firma L e y b o 1 d - H e r a e u s entspricht der Abstand von 1,5 cm bei den Kalottenmodellen 1 •. Die Molekiilbilder wurden ausgeschnitten und dann der Schwerpunkt dieser Bilder ermit- telt. Durch den Schwerpunkt wurde eine sog. Hauptachse (W-O-Richtung) und von diesem aus von 0 ø his 360 ø alle 10 Grade Linien gezogen die Hauptachse muB in jedem Bild iibereinstimmen, damit auch die 10 Grad-Linien deckungsgleich sind, die zur
Purchased for the exclusive use of nofirst nolast (unknown) From: SCC Media Library & Resource Center (library.scconline.org)